
提到热量限制(Caloric Restriction, CR),人们常常将其与“减肥”挂钩。但眼光不要这么局限嘛,CR带来的好处可远不只减重!
大量研究证实,在充分保证营养成分(如必需氨基酸、维生素等)的情况下,限制每日摄取的总能量,真的能改善健康状况,甚至达到“续命”目的。
不过,关注CR研究的人都有这样的感受,先前的实验大多基于动物而非人类。啮齿类动物实验证明,40%的CR模型能诱导负能量平衡,以抑制炎症、减轻疾病负担,从而达到延长小鼠寿命的作用。
但这样的CR模型真的能类推到人类吗?40%的热量限制,续不续命倒不重要,可能先“饿不活”了!
为了测试CR在人类身上的可行性、揭示其带来健康好处的背后机制,来自耶鲁大学的研究团队对CR的参与者进行了基因分析,并与正常进食组进行了比对。结果发现,CR能减少人体内一种名为SPARC的基质细胞蛋白的产生,从而抑制有害炎症、改善代谢功能,延长老年时的健康寿命。该研究是首个在健康人类中开展的CR随机对照研究,于8月12日发表在Cell子刊Immunity上。

在开展试验前,研究者首先思考的问题是:若将小鼠中的40%CR模型推广到人类,岂不是太极端了?对人类的热量限制要控制在多少,是可接受且最可控的?
基于先前长达2年的大型热量限制RCT临床试验(Comprehensive Assessment of Long-term Effects of Reducing Intake of Energy, CALERIE-II),研究者发现,在自由生活的条件下,14%的CR是人类可接受的,且能有效降低血液中的炎性标志物。
以一个正常人为例,如果这个人每日摄入的能量为1800kcal,14%的CR即252kcal,约等于一只冰淇淋、1/2个巧克力牛角面包、50g薯片、一个小奶油蛋糕等等。也就相当于砍掉每日零食,还是很好接受的。
为进一步评估CR的长期影响及内部机制,研究者将参与者分为两组:试验组在2年内每天减少14%能量摄入,而对照组每日正常进食。在基线、试验进行了1年和2年的时间点,提取参与者的腹部皮下脂肪组织进行RNA测序,来探究CR引起的基因变化。
结果显示,①在经过1-2年的CR后,试验组的脂肪组织中SPARC显著下降,且与BMI、体脂率、瘦素、C反应蛋白(CRP)、肿瘤坏死因子-α(TNFα)、整合蛋白ICAM-1的降低有关。②相反,与相对苗条的相比,肥胖个体中SPARC蛋白的含量更高。
综合上述两个结果,研究者推测,SPARC很可能是“损害人体健康”的幕后BOSS蛋白,会导致与肥胖相关的炎症增加。
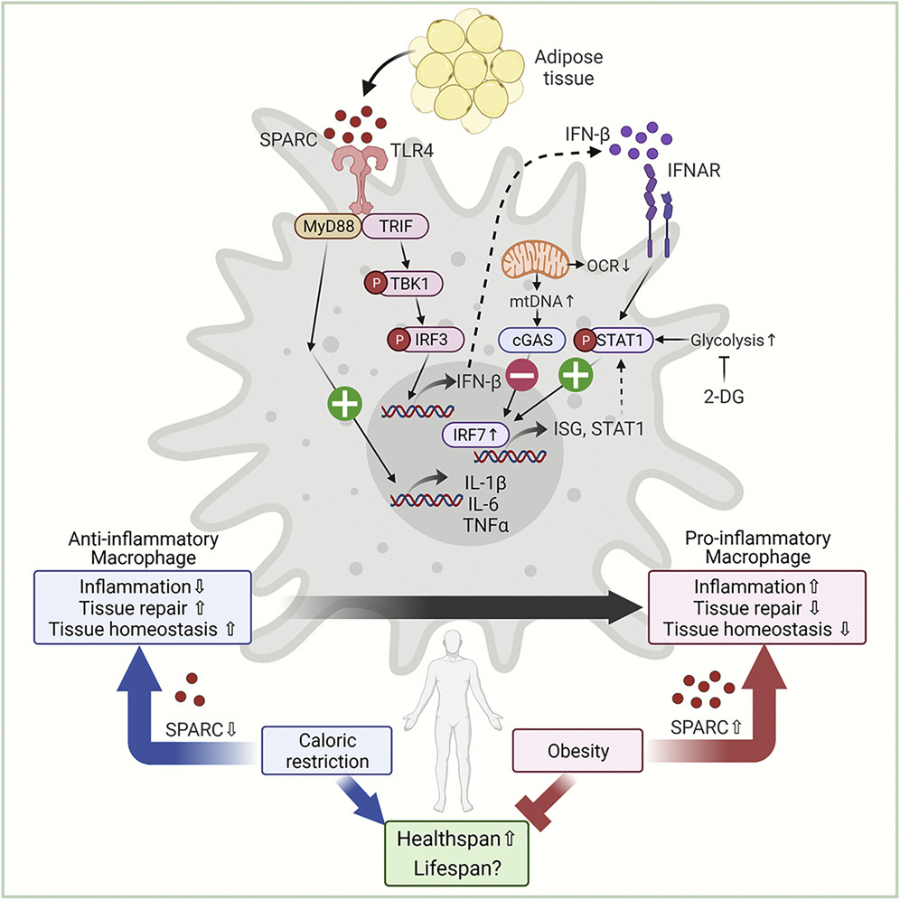
人体内SPARC蛋白途径
SPARC,何许蛋白也?SPARC是Secreted protein acidic and rich in cysteine的缩写,即一种富含半胱氨酸的酸性分泌糖蛋白,与肥胖、糖尿病、炎症的发生有关。
“充分的研究证明,炎症在年龄相关的衰退中起到了重要作用。但像CR这样的干预措施,是如何通过SPARC来发挥控制炎症的作用呢?”为进一步弄清楚背后的机制,耶鲁大学Vishwa Deep Dixit教授团队建立了小鼠模型。
不出所料,小鼠体内的SPARC蛋白通过糖酵解和IRF7诱导巨噬细胞中的干扰素反应,并通过激活TLR4将原本抗炎的M2巨噬细胞转化为促炎表型M1巨噬细胞,从而促进了炎症的发生,造成健康损害。
当研究者对比SPARC脂肪细胞缺陷小鼠与正常对照组时发现,降低小鼠脂肪细胞产生的SPARC蛋白,不仅改善了其葡萄糖耐量和胰岛素敏感性,更重要的是,实验组老年小鼠的虚弱程度明显降低(体现在老年小鼠焕发生命活力,不仅握力增强,还能在旋转杆上狂奔,堪称医学奇迹啊)。
很显然,在限制SPARC产生的情况下,老年小鼠体内由衰老引起的代谢失调得到了缓解,使其健康寿命得到了延长!
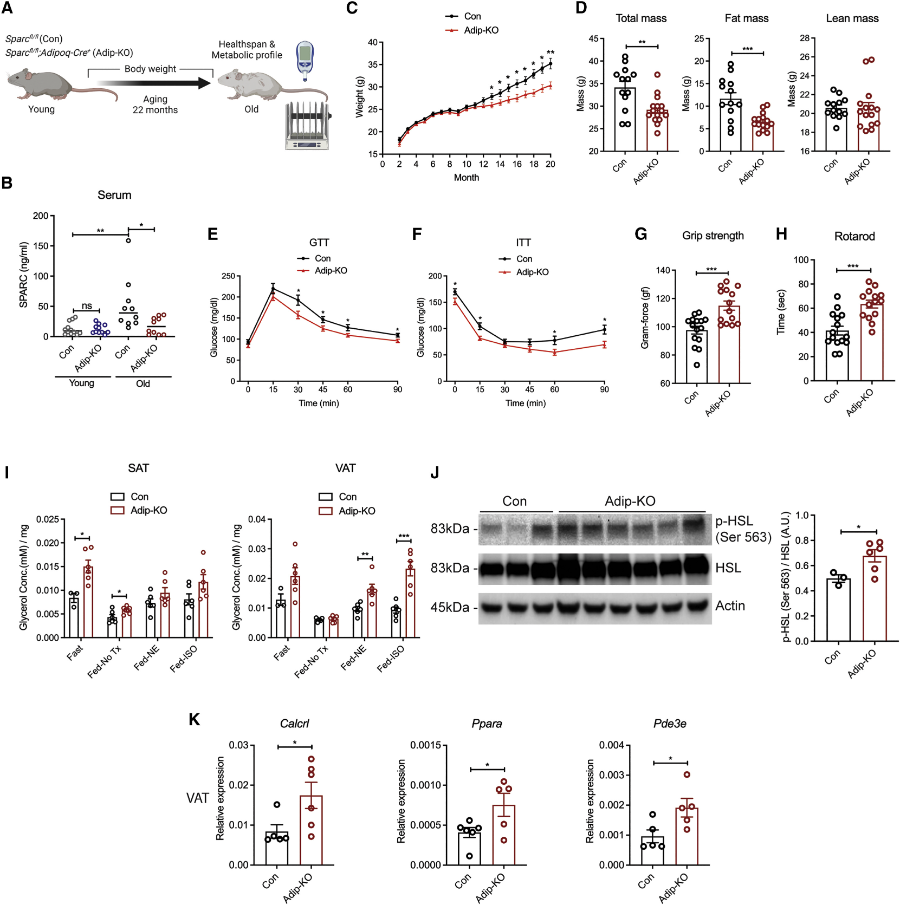
抑制SPARC可减少年龄相关的炎症增加
欸,换句话说,限制能量摄入是为了减少SPARC蛋白的产生,从而抑制有害炎症,延长老年健康寿命。整个过程中,SPARC才是那个诱发炎症“罪魁祸首”。
那么,在实际运用中,可不可以在不改变卡路里摄入量的情况下,仅诱导SPARC降低而实现续命呢?这也是研究人员下一步的研究重点。如果真能实现“不用挨饿也能长寿”,岂不美哉?
不过,在现阶段(在研究没有进展到下一步之前),我们只能每天少吃一口零食,在享“瘦”的同时,也为自己的老年续上“高质量”命吧~
作者:Swagpp
编辑:顾军
责任编辑:姜澎
转载:梅斯医学
声明:转载此文是出于传递更多信息之目的。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。





