相关文章
推荐文章
排行榜
刚刚!四个新型冠状病毒检测产品获批上市,其中两家企业来自上海
日期:2020年01月26日 22:51:42 作者:沈湫莎
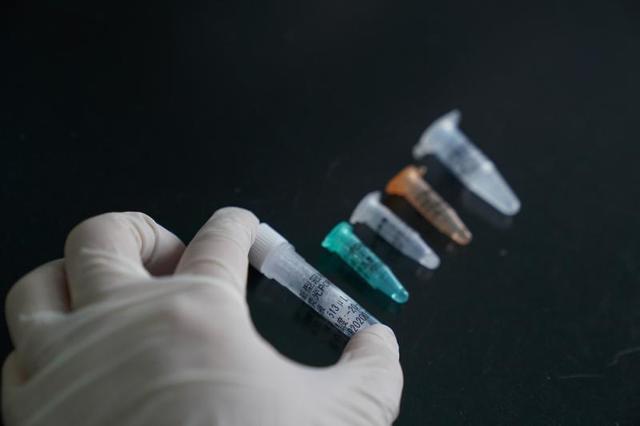
国家药品监督管理局今天应急审批通过四家企业四个新型冠状病毒检测产品,进一步扩大新型冠状病毒核酸检测试剂供给能力,全力服务疫情防控需要。四家企业中有两家上海企业,分别是之江生物和捷诺生物。
之江生物所研发的检测试剂盒的科学原理名为“荧光PCR(聚合酶链式反应)法”,它是一种用于放大扩增特定DNA(脱氧核糖核酸)片段的分子生物学技术,能利用聚合酶链式反应将微量的DNA大幅扩增,从而检测出带有特定基因片段的病毒。
捷诺生物检测试剂盒的检测方法主要是从样本中提取核酸后加入扩增检测试剂,若存在病毒基因,试剂中的反应体系会将其进行指数级扩增,从而将病毒基因高效表达出来。阳性样本会通过荧光检测,进一步判断患者是否被感染。
“哪里需要送哪里,全力以赴与疾病赛跑。”捷诺生物市场部相关负责人表示,春节期间安排专门的管理人员负责生产、质量、储运方面的监控和应急值守,保证生产安全有序进行。上海之江生物科技股份有限公司研发负责人也表示,公司已经加班加点生产检测试剂盒,日产量20万人份,尽可能满足市场对检测试剂盒需求。
疫情发生后,国家药监局立即启动医疗器械应急审批程序,按照“统一指挥、早期介入、随到随审、科学审批”的原则和确保产品安全、有效、质量可控的要求,全力加快审评审批速度。据悉,国家药监局仍将继续对疫情防控所需的药品医疗器械采取特殊审批程序,争取相关产品尽快上市。
作者:沈湫莎
编辑:张鹏
责任编辑:任荃
*文汇独家稿件,转载请注明出处。
文汇网 ● 版权所有 All Rights Reserved ICP许可 沪 B2-20150001 号 Copyright(c)2004 沪公网安备 31010602000205号





