
记者从今天的顶尖学术期刊《自然》看到一篇论文,报告了一项在全世界备受关注的田间试验结果。科学家们在摘要中指出,结合两种改造蚊子的技术,在中国广州的试验现场,他们将世界上最具侵略性的一种蚊子的种群“几乎完全消灭”(near elimination)。这项传染病控制领域的成功得到了《自然》的专题报道。

他们将世界上最具侵略性的一种蚊子的种群“几乎完全消灭”
被灭的蚊子就是我们非常熟悉、更是十分痛恨的白纹伊蚊(Aedes albopictus),俗称“花脚蚊子”。它们原产东南亚,遍布全世界,被入侵物种专家小组列为世界百大外来入侵种之一。
白纹伊蚊之所以遭人恨不仅仅是因为送我们的“红包”非常痒,更是因为它们传播很多疾病,包括登革热、疟疾、黄热病、基孔肯雅热、寨卡,等等。
▲俗称“花脚蚊子”的白纹伊蚊
科学家们与传播疾病的蚊子做出了长期斗争,尝试过不少方法来压制蚊子的种群数量。比如,有一种策略是利用辐射让雄蚊不育,再把它们放到野外。因为白纹伊蚊只有雌蚊吸血,雄蚊吃素(取食植物的汁液),所以投放出去的雄蚊对人类没什么影响,又可以干扰雌蚊产下后代。但是后来发现,不育雄蚊通常比较虚弱,相比野生雄蚊,难以吸引雌蚊子。因此光靠这种“昆虫节育技术”,控蚊效果还不理想。
另一个更好的方法是用一种叫“沃尔巴克氏体”(Wolbachia)的细菌感染蚊子。这种细菌对人体无害,但能感染很多昆虫,并影响昆虫的生殖细胞。受到细菌感染的雄蚊子释放到野外后,当它们与未受感染的雌蚊子交配时,有沃尔巴克氏体的精细胞遇到不含同种细菌的卵细胞,“胞质不融合”现象会让虫卵无法存活,达到让蚊子绝育的效果。
细菌感染的方法在小规模试验中确实效果很好,可以把蚊子完全消灭。然而在更大范围实施时,存在一个风险:研究者要把感染了沃尔巴克氏体的雌蚊挑出来消灭,漏网雌蚊被放到野外的话,还能继续产下后代,并取代野外蚊子的种群。
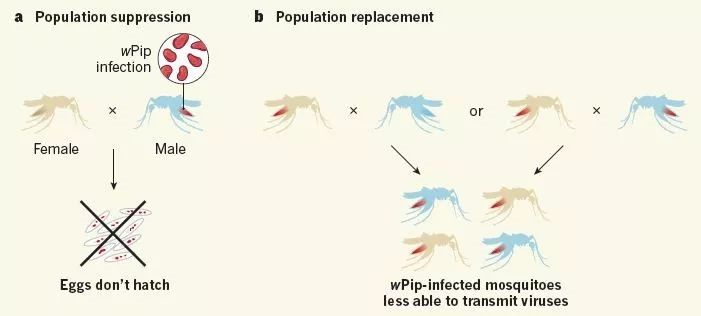
▲感染沃尔巴克氏体的雄蚊子会让未感染的雌蚊子无法产生可孵化的虫卵;但感染沃尔巴克氏体的雌蚊子可能让整个种群都带上同种细菌
在中山大学与密歇根州立大学联合创立的热带病虫媒控制联合研究中心,负责人奚志勇教授带领的研究队伍将上面两种方法做了组合和优化。具体来说,科学家们首先让白纹伊蚊感染三种沃尔巴克氏体菌株,保证雄蚊和野生雌蚊交配时会发生胞质不融合而让蚊子绝后。
随后,研究人员结合了低剂量辐射让蚊子不育。这么做的好处是,被细菌感染的雌蚊即便意外放出去也没有风险,同时保证辐射水平不至于影响雄蚊的生殖竞争力。科研人员减轻了筛选蚊子雌雄的压力,养蚊子的“蚊子工厂”产量大增,每周可以产生500万只改造的雄蚊子!
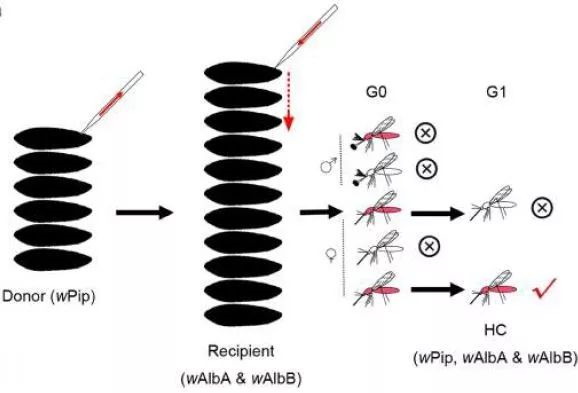
▲利用显微胚胎注射技术,从其他蚊子体内提取一种沃尔巴克氏体,导入已有两种菌株的白纹伊蚊体内,筛选出与三个菌株有共生关系的蚊子品系
经历了双重改造的白纹伊蚊,可以帮助控制野外的种群,有效减少登革热等疾病的传播吗?
经过实验室内的小规模成功,以及对种群数量变化的理论推演后,研究团队经农业部批准,展开了“以蚊治蚊”的开放式田间试验。研究团队与广东省和广州市的疾控中心合作,选择了两个相对隔离的小岛,从2015年开始投放大规模培育的“绝育”蚊子。
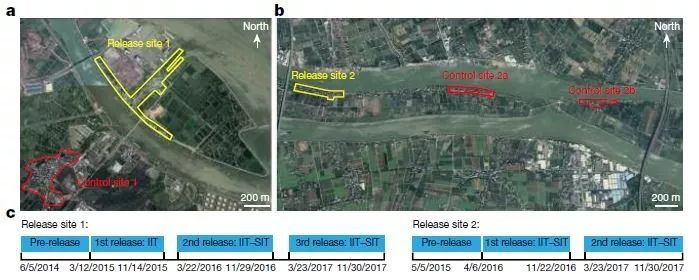
▲研究人员选择了广州的沙仔岛和大刀沙作为试验点,2015年在沙仔岛释放了只经过细菌感染的雄蚊,2016和2017释放了经过双重改造的雄蚊
在2016年和2017年,蚊子的繁育季节,每周、每公顷有16万只既受过三重细菌感染又受过辐射的白纹伊蚊登场。在随后的时间里,科学家们每周监测蚊子卵的数量和成体雌蚊子的数量变化。
正如科学家们的预期,控制效果十分喜人!持续两年,在释放蚊子的试验点,相比对照地点,野生蚊子数量锐减90%左右!
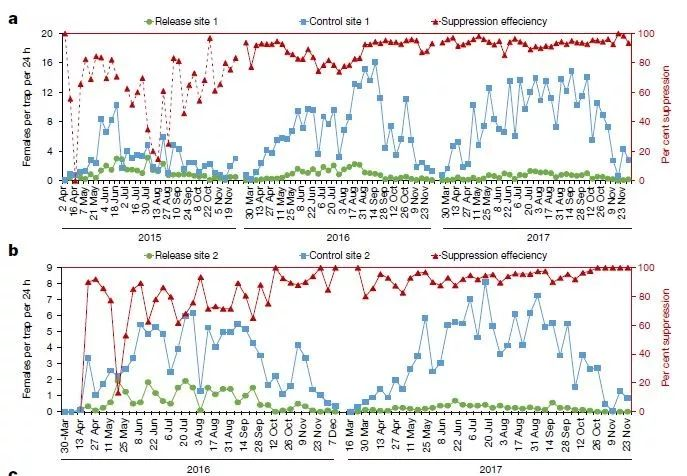
▲两个试验点野生型成年雌蚊的平均数量减少83%~94%,长达6周内都侦测不到任何蚊子
种群遗传学分析显示,仅剩的蚊子可能是从研究地区之外的地方随着人类活动迁移进来的。
值得一提的是,蚊子数量的大幅减少也从岛上居民的直观感受中反映出来。两个岛上,蚊子的叮咬率分别下降了96.6%和88.7%!不被蚊子叮,自然就不容易感染蚊子传播的疾病,这无疑是控制蚊媒疾病传播的有力佐证。
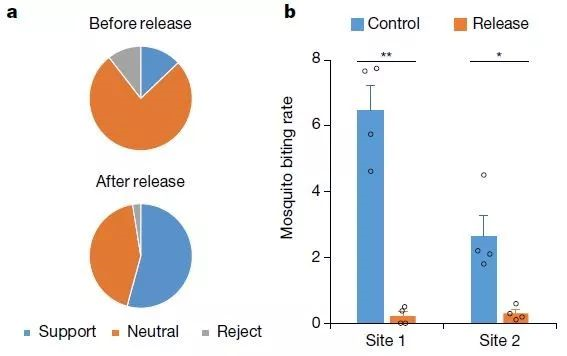
▲蚊子的叮咬率大幅下降,岛民们对投放蚊子的支持率从试验前的13%提高到试验后的54%
为了阻绝蚊子传播的各种疾病,科学家们一直在尝试各种方法。
比如研究人员通过一种转基因真菌,安全地将一种毒素传递给蚊子,从而使蚊子的数量减少了99%以上。这一研究也登上了《科学》杂志。
该项目的灵感,源自于真菌孢子可以落在昆虫体表、最终感染或杀死其宿主的观察实验。不过就效率而言,真菌孢子并不是杀灭蚊子的最佳方法。
在现实世界,通常需要很多孢子,才能达成预期的效果。有鉴于此,研究人员致力于增强一种名为绿藻(Metarhizium Pingshaensei)的真菌的毒性。
据悉,这是一种携带疾病的蚊子的自然杀手,冈比亚按蚊(Anopheles Gambiae)和埃及伊蚊(Aedes Aegypti)都不是它的对手。
经过基因改造,这种真菌可以表达自北非沙漠蝎子和澳大利亚蓝山漏斗网蜘蛛的毒素。
先前试验表明真菌可有效杀死目标蚊子,但更重要的是,该真菌的感染能力极具针对性、不过丢蜜蜂等其它物种产生危害。
研究合著者 Raymond St. Leger 表示:“这些真菌具有很强的选择性,它们知晓来自昆虫的独特体征,而我们也特地选用了亲蚊的菌株”。
当这种真菌检测到自己已经附着在蚊子身上时,就会穿透并进入蚊子的角质层。更棒的是,它不会给包括蜜蜂在内的其它昆虫带来麻烦或安全隐患。
据悉,本轮研究选择了在疟疾流行的布基纳法索农村地区的户外受控环境中展开测试,且研究人员们建造了一座名叫 MosquitoSphere 的大型的筛选设施。
该设施内部构建了三个小屋,分别对应三种不同的模拟场景 —— 其中一个小屋不含真菌,另一个含有非工程真菌,第三个则部署了基因工程真菌。

然后,研究人员在每个小屋内释放了1000只成年雌性/500 只成年雄性蚊子。在接下来的45天内,研究人员会每天清点昆虫的数量。
最终,身处转基因真菌小屋的成年蚊子只有13只存活,显然已经低于种群繁衍所需的数量。作为对比,非工程真菌小屋里仍有455只成年蚊子存活,无真菌小屋里更是增加到了1396只。
论文第一作者Brain Lovett 解释称:只需将转基因真菌挂在研究区墙上的薄片,就可以让蚊群数量在45天内出现崩溃,意味着它在灭杀具有抗药性的蚊子的效果上,与灭杀无抗药性蚊子具有同样的效果。
接下来,研究团队希望在当地村庄或社区进一步测试他们的转基因真菌。当然,在将这种新方法应用于开放环境(如村庄) 之前,需要满足许多监管,而研究人员表示,现在的这一研究结果有助于为此类开放环境试验提供一定依据。
编辑:沈湫莎 陈孙杰(实习生)
责任编辑:姜澎
来源:学术经纬、蝌蚪五线谱、DeepTech深科技





