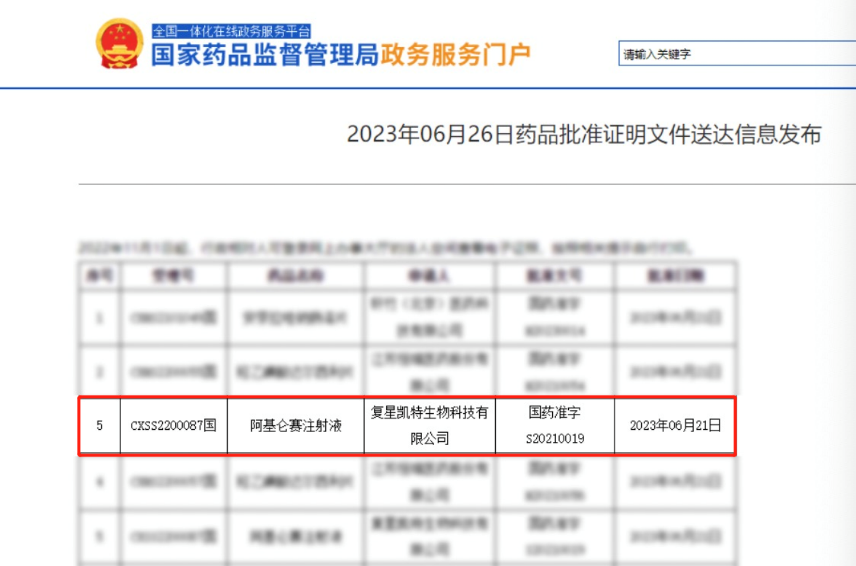
中国淋巴瘤患者迎来新希望。根据国家药监局官网消息,近日,阿基仑赛注射液(奕凯达)用于治疗一线免疫化疗无效或在一线免疫化疗后12个月内复发的成人大B细胞淋巴瘤上市注册申请获国家药品监督管理局附条件批准。这标志着这一CAR-T细胞治疗产品二线适应症正式上市,奕凯达也成为目前国内首款获批的用于本次新增适应症的CAR-T细胞治疗产品。
此前,中国境内尚无用于治疗一线免疫化疗无效或在一线免疫化疗后12个月内复发的成人大B细胞淋巴瘤的CAR-T细胞治疗产品,复星凯特奕凯达新增二线适应症的获批上市,成功推进了治疗进展,为更多一线免疫化疗无效或复发的患者带来希望。
“最新调研显示,淋巴瘤在我国的发病率逐年递增,如何改善淋巴瘤治疗预后、提高临床治愈率,备受业界关注。”哈尔滨血液病肿瘤研究所马军教授表示,所有肿瘤药品都是从末线适应症开始突破,获批后继续推进二线或一线适应症的获批,就是因为治疗端口的前移才能带来更大、更彻底的患者获益,这是新药研发的规律。
马军同时谈到,中国医药行业正在蓬勃发展,从企业到监管等多个维度都在尝试进行创新,奕凯达二线治疗成人大B细胞淋巴瘤适应症在中国的快速获批,是CAR-T细胞治疗领域新的里程碑,也是中国淋巴瘤患者的巨大好消息。
成人大B细胞淋巴瘤是常见的恶性淋巴瘤,具有治疗方案少、病情进展快、死亡率高等特点,近年来在中国的发病率呈快速增长趋势。2021年6月,复星凯特率先上市国内首个CAR-T细胞治疗产品——阿基仑塞注射液,2021年6月至今,其以个性化定制、一次性疗法已惠及超过500位复发/难治性大B细胞淋巴瘤患者。
复星凯特CEO黄海表示,奕凯达新增二线适应症的获批上市,是复星凯特在解决淋巴瘤患者未被满足的重大医疗需求道路上迈出的关键一步,更是凝结着我国药品审评审批部门在创新药审批监管方面的巨大努力和心血。
作者:唐闻佳
编辑:储舒婷
责任编辑:姜澎
*文汇独家稿件,转载请注明出处。





