对中国广大癌症患者而言,2018年无疑是令人激动的一年,多款革命性抗癌药物集中上市,其中备受瞩目的就是默沙东的PD-1抗肿瘤药物帕博利珠单抗注射液Keytruda,即大家熟知的“K药”。
昨天傍晚,国家药品监督管理局正式批准K药联合化疗用于非鳞状晚期非小细胞肺癌(NSCLC)的一线治疗,且无需考虑患者组织样本的PD-L1表达状态。
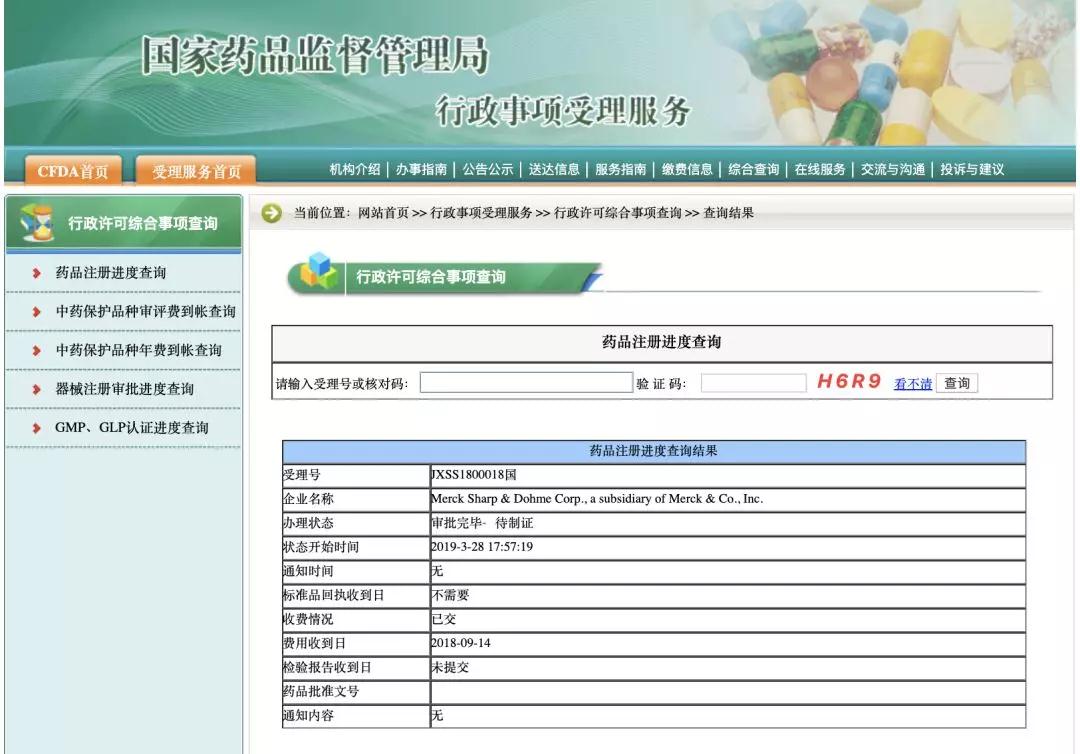
▲官网显示,K药联合化疗用于非小细胞肺癌的一线疗法注册申请(JXSS1800018)进度已变更为“审批完毕 待制证”,这也意味着K药在中国的第二个适应症已正式完成审批,进入最后制证阶段。
去年7月25日,K药正式通过中国药品监督管理局批准上市,用于晚期黑色素瘤治疗,创下中国进口抗肿瘤药物最快审批记录。
而此次K药NSCLC适应症的获批比黑色素瘤意义更大,因为肺癌患者群体数量远超黑色素瘤患者。
目前全球仅有Keytruda和Tecentriq两种药物获批为NSCLC的一线疗法。
K药将开启NSCLC一线治疗新时代
在我国,肺癌的患病率及死亡率均居恶性肿瘤榜首。NSCLC是肺癌的主要类型,占全部肺癌患者的85%。其中非鳞状NSCLC占70%,更为难治的鳞状NSCLC占30%。
根据Global Data数据,2015年全球NSCLC患者中有46%在中国,到2020年,这个比例会增高至62%。其中,不能接受靶向治疗的非鳞状非小细胞肺癌患者只能选择化疗、放疗等传统治疗方法,不仅治疗手段有限,生活质量难以保证。
每年数十万的肺癌患者苦等新药的出现,肺癌领域存在着巨大未被满足的需求。如今,K药联合化疗的获批给这些患者带来了新希望。
据悉,K药本次获批是基于代号为KEYNOTE-189的临床试验,KEYNOTE-189研究是免疫检查点抑制剂联合化疗用于NSCLC一线治疗的第一个国际多中心双盲、安慰剂对照III期临床研究。
作为一项III期临床试验,入组的患者为EGFR或ALK阴性的晚期非鳞非小细胞肺癌,实验组的病人使用K药联合培美曲塞和顺铂或卡铂,对照组病人使用培美曲塞联合顺铂或卡铂。
试验结果表明不管是总生存期还是无进展生存期,K药联合化疗都远远胜出当前的标准治疗方案。

▲总生存期(OS):联合组一年生存率为69.2%,化疗组仅为49.4%。
从KEYNOTE-189研究结果可以看出,K药联合化疗治疗非鳞NSCLC可以带来比标准化疗更大的生存获益;对于符合条件的NSCLC患者,K药用得越早,生存获益就越大,K药联合化疗是一个更好的选择。
更多扩大适应症范围的临床试验正在进行
作为首个在中国获批的PD-1免疫疗法,K药时隔8个月后再次成功获批新适应症,亦成为首个免疫联合疗法获批肺癌一线治疗的药物。
从全球范围获批适应症数量来看,K药已在80多个国家获批使用,覆盖了9个癌种的12个适应症,包括黑色素瘤、非小细胞肺癌、头颈癌、霍奇金淋巴瘤、膀胱癌、子宫颈癌、胃癌等多个癌种。
值得一提的是,2017年5月,K药被革命性地批准上市用于治疗MSI-H(微卫星不稳定性高)实体瘤,这是FDA批准的首款不依照肿瘤来源,而是依照生物标志物进行区分的抗肿瘤疗法,成为第一个真正意义上的广谱抗癌药。

目前除黑色素瘤和非小细胞肺癌外,K药在中国还启动了食管癌、肝癌等临床试验,未来或有更多适应症获批。
不过值得注意的是,虽然从理论上讲,PD-1和PD-L1的作用机理大致相同,然而,从细微的作用机理上看还是有差别的。
随着国内越来越多免疫治疗药物获批,患者在使用时一定要考虑每一款药物获批的适应症是什么,一定根据自身具体情况和医生多沟通,遵医嘱用药,不能随意更换。
作者:记者 李晨琰
编辑:顾军
责任编辑:唐闻佳
*文汇独家稿件,转载请注明出处。





