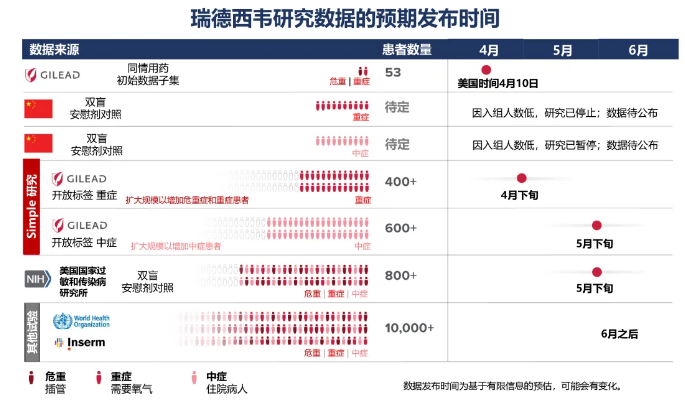
瑞德西韦各项试验的汇总和预期的数据公布时间。图源:吉利德科学微信公众号
北京时间4月24日凌晨,英国《金融时报》报道称,一份世卫组织意外公布的文件草案显示,瑞德西韦在治疗新冠病毒的首个随机临床试验(中国第一个临床研究)中失败。
针对外界关于治疗新冠潜在有效药物瑞德西韦有效性的质疑,吉利德公司作出回应。
美国时间4月23日,吉利德科学全球首席医疗官Merdad Parsey博士代表公司,发布了吉利德科学关于瑞德西韦针对新型冠状病毒肺炎重症患者在中国的研究数据的声明。
声明称,“今天,世界卫生组织(WHO)网站上过早地发布了中国第一个临床研究的信息,该研究评估了在研抗病毒药物瑞德西韦(remdesivir)在新型冠状病毒肺炎重症患者中的使用。这一信息已经被删除,因为研究人员并未许可公布结果。此外,我们认为那篇文章包含了对研究的不恰当描述。由于入组率低,该研究被提前终止,因此,它的数据不足以支撑有统计意义的结论。就其本身而言,该研究结果是非结论性的,尽管数据的趋势提示了瑞德西韦的潜在受益,尤其是在早期接受治疗的患者中。我们获悉现有的数据已经提交用于经同行评审的发布,近期将会看到这项研究的更详细的信息。”
据英国《金融时报》报道,中国的临床试验显示,瑞德西韦并没有改善患者的病情,也没有减少病原体在血液中的存在。研究者对237名患者进行了研究,给158名患者服用该药,并与其余79名患者的进展进行对比。另外,该药也在一些人身上出现了明显的副作用,这意味着18名患者被停药。
世卫组织表示,这份正在接受同行评审的文件草案错误地过早发表。“为了回应世卫组织要求提前分享信息和研究的要求,一份由作者提供的文件草案被提供给了世卫组织,并且不经意地发布在了网站上。在发现错误后,该文件即被撤下。”
据悉,4月10日,吉利德科学公司董事长兼首席执行官丹尼尔·奥戴(Daniel O’Day)在官网发表了一封公开信。信中称,中国已经停止重症临床试验,另外,瑞德西韦同情用药的数据存在局限性。
据澎湃新闻报道,查询临床试验网站clinicaltrials.gov显示,瑞德西韦在中国新冠肺炎成人重症试验状态为“终止”,原因显示为:“中国新冠肺炎疫情已经得到良好控制,当前没有符合条件的患者入组。”
同时,瑞德西韦在中国的新冠肺炎成人轻症和中度症状组的临床试验状态也已更新为“暂停”,原因显示为:“当前,新冠肺炎疫情已得到良好控制,没有符合条件的患者入组。”
吉利德在官方声明中表示,这项在中国的试验结果,以及4月19日公布的更多重症病人同情用药的结果为瑞德西韦增加了研究证据,但仍无定论。
声明同时提及,多个正在进行中的三期研究将提供额外的数据,以确定瑞德西韦作为新型冠状病毒肺炎治疗药物的潜力。这些研究将有助于明确使用瑞德西韦的治疗对象、治疗的启动时间以及持续时间,研究有的已经完成初级分析所需的全部入组,有的按照计划即将完成入组。
根据吉利德科学方面预期,本月底将发布针对瑞德西韦用于新冠肺炎重症患者的开放标签研究的结果。这是一项随机的临床试验,已经完成全部的患者入组,研究将比较使用瑞德西韦5天或10天后的治疗结果和安全性。
“我们预期在五月底获得对中症患者的开放标签研究数据,该研究将对比患者使用瑞德西韦5天、10天以及接受标准治疗的结果。我们预计,五月底还可以获得美国国家过敏和传染病研究所(NIAID)对不同严重程度的患者进行的瑞德西韦双盲、安慰剂对照研究的数据。”声明表示。
编辑:苏展
责任编辑:施薇





