《美国科学院院报》在线发表瑞金医院沈柏用团队胰腺癌相关最新研究成果
胰腺癌被称为“癌中之王”,死亡率高,发病率也在升高。现有治疗手段有限,急需医学科研上的突破。
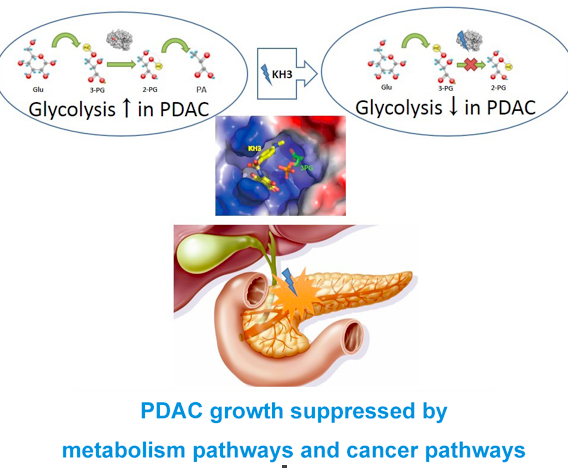
10月29日,《美国科学院院报》(PNAS)在线发表上海交通大学医学院附属瑞金医院沈柏用团队胰腺癌相关最新研究成果。该研究首次发现抑制糖代谢通路关键调控蛋白磷酸甘油酸变位酶1(PGAM1)能有效杀灭胰腺癌细胞,该研究在胰腺癌的多种临床前模型(原代细胞、原位植入模型、PDX模型等)中证实了PGAM1新型别构抑制剂(命名为:KH3)对胰腺导管腺癌的抑瘤作用,为胰腺癌的精准治疗开启了“靶向抑制肿瘤代谢通路”的新篇章。

PGAM1是糖酵解通路中的关键代谢酶,其催化糖酵解通路中的3-磷酸甘油酸(3-PG)转化生成2-磷酸甘油酸(2-PG),促进葡萄糖代谢和能量生成,通过调节3-PG与2-PG的转化平衡来影响其他代谢通路,并参与细胞内生物大分子合成和维持氧化还原稳态,促进肿瘤细胞增殖。
胰腺导管腺癌(PDAC)被称为“癌中之王”,死亡率极高,全球长期存活率在所有实体瘤中持续最低,而其发病率在逐年提高,预计至 2030 年胰腺癌将居癌症死亡原因第二位,严重威胁人类健康。
针对胰腺癌,根治性手术切除是唯一有效的根治手段,然而大部分患者在确诊时已无根治手术机会,胰腺癌的综合治疗是大多数胰腺癌患者的首选方案。目前的主流治疗手段有放化疗、分子靶向治疗及免疫治疗等,但治疗效果仍不尽如人意,因此发现胰腺癌新的治疗靶点或治疗策略迫在眉睫。
代谢异常是胰腺导管腺癌的主要特征之一,本研究发现PGAM1在胰腺导管腺癌患者 (PDAC)中高表达,且与临床预后正相关。
研究团队根据以往工作,通过共晶结构解析对先导化合物进行优化、改造,得到了一种新型的PGAM1别构抑制剂KH3,其具有高选择性、高活性、低毒性等优势。KH3与PGAM1邻近底物结合口袋的别构位点相互作用,抑制3-PG向2-PG转化,显著降低PGAM1的代谢活性。

沈柏用教授团队
研究人员发现,KH3可显著抑制PDAC细胞系及原代细胞增殖,且抑制效果与PGAM1表达量相关。
同时,课题组也通过转录组学分析发现,PGAM1抑制剂可协同抑制多个肿瘤代谢通路及肿瘤发生的经典通路,肿瘤代谢、发生通路的抑制程度也可提示药物应答效果。
沈柏用教授分析,KH3可在多个胰腺癌临床前模型中有效抑制肿瘤生长,特别是在PGAM1高表达模型中更为显著,且药物毒性可被耐受。这预示着PGAM1抑制剂具有转化为临床药物的巨大潜力,且抑制肿瘤代谢通路可作为胰腺癌未来治疗的重要方向。
该工作联合复旦大学药学院、国家转化医学中心和奥克拉荷马大学健康科学中心合作完成。复旦大学药学院周璐副教授,上海交通大学医学院胰腺疾病研究所沈柏用教授、方圆副研究员,奥克拉荷马大学健康科学中心李敏教授和国家转化医学中心陈竺院士为该论文共同通讯作者。
上海交通大学医学院附属瑞金医院温晨磊医师、复旦大学药学院2013级博士研究生黄科、2016级硕博连读研究生江露露和瑞金医院陆熊熊医师为论文共同第一作者。
该研究受到国家自然科学基金、上海市科委基金、上海市教育委员会科研创新重点项目及上海市东方学者等项目支持。
作者:唐闻佳
编辑:储舒婷
责任编辑:唐闻佳
*文汇独家稿件,转载请注明出处。





